在线客服
在线客服
医疗器械注册人制度颠覆医疗器械行业
医疗器械注册人制度允许医疗器械注册申请人可以是医疗器械企业、研发机构、科研人员、医生专家等主体,激发了医疗器械行业的创新和创业热情。
该制度允许医疗器械注册人将生产委托给多个有资质和生产能力的企业,极大地便利了具有研发能力的人员和机构的技术转化,有利于科研成果的转化输出和创新产品的上市。
医疗器械注册人制度要求注册人对医疗器械设计开发、临床试验、生产制造、售后服务等全生命周期产品质量承担全部责任的制度,促进产业发展的同时也明确了注册人的权利与义务,有利于监管机构有效监管。
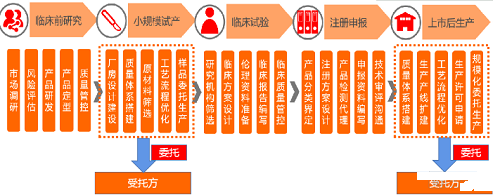
(医疗器械生产流程及委托生产介入环节)
医疗器械注册人制度中关于委托生产模式的规定促进了行业精细化分工。该制度允许注册人多点委托生产,使企业不再必须自建厂房。这将使擅长研发的只需专注研发,擅长生产的只需专注生产,大大提高了行业资源利用率,对于企业创新和产业升级有巨大帮助。另外,委托生产模式将在医疗器械的某些细分领域促进医疗器械研发机构与制造企业更趋向于精细化分工合作,优化行业资源配置。
医疗器械注册与生产“解绑”,降低了医疗器械行业的进入门槛。资本、创业者、社会资源等在医疗器械注册人制度下进入医疗器械行业更为便捷。这不仅扩大了医疗器械行业的市场规模,也提升了资源的利用率。
医疗器械注册人委托生产模式详解
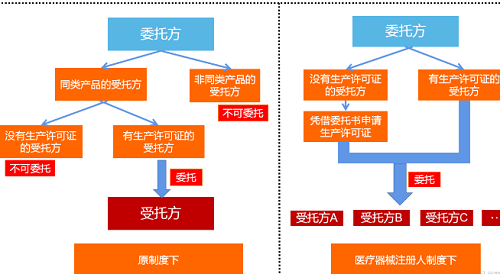
在医疗器械注册人制度实施前,委托生产模式需要委托方与受托方均拥有同类产品生产许可证。如下图所示,委托方必须委托有同类产品注册证书及同类产品生产许可证的企业。但是,可以生产同类产品的企业一般而言是竞争对手,另外,两家均具备了同类医疗器械生产许可证的企业从软硬件资源配置上趋同,委托生产业务产生的必要性和可行性较小。
医疗器械注册人制度下,医疗器械注册人既可以自行生产,也可以委托单个或多个企业生产。在委托生产中,有资质的受托方可直接进行生产,受托方也可凭借注册人的委托书申请生产许可证,从而进行受托生产。如此一来,受托方不需要具备医疗器械注册证也可从事生产,真正实现注册证与生产许可证的分离,有利于行业资源配置,便于企业专注于擅长的事。
医疗器械注册人制度最新发展
据了解,《医疗器械监督管理条例》目前还处于修订过程中,预计在今年下半年发布的机会较大。本次《医疗器械监督管理条例》修订的一项主要任务就是把医疗器械注册人制度写入条例,确立医疗器械注册人制度的法律地位。
医疗器械注册人制度写入《医疗器械监督管理条例》,这将对行业的发展产生颠覆式的变化。
第一,目前国内医疗器械创新不足,企业对于产品创新的动力不足,在医疗器械注册人制度下,临床医生、专家及科研医工人员的创新项目将更易于商业化,可以加速医疗器械行业的创新。。
第二,医疗器械注册人制度下,创新企业可以专注研发,将法规、注册、临床试验、生产、品牌、销售等问题委托给行业内相应的第三方专业服务机构即可,行业内也有望实现医疗器械从研发到上市每一个环节的细分化外包市场供需关系,真正实现“让专业的人做专业的事”。
第三,医疗器械注册人制度降低了创新和创业门槛,初创企业无需自建工厂,减少了投入成本,有了更多发展机会。
第四,医疗器械注册人制度将有望利用中国业已具有的巨大的市场、良好的产业链配套、逐步完善的监管和知识产权保护制度,吸引更多、更好的国际创新技术研发和制造中心落地中国。
广州安思泰企业管理咨询有限公司目前公司已服务800多家客户。公司的服务得到客户的一致好评,并且成为了长期的合作伙伴。为医疗器械生产企业、经营......
经过我司专业的辅导已经客户的积极配合,4个月顺利获得医用口罩注册证。......
为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,国家药品监督管理局组织制定了《有源医疗器械使用期限注册技术审查指导原则》,现......
为贯彻落实党中央国务院和省委省政府减税降费政策措施,切实减轻企业负担,优化营商环境,决定降低海南省药品注册与医疗器械产品注册收费标准,已于6......
通过我司专业的辅导,客户顺利通过药监部门的现场审核,顺利取得三类医疗器械经营许可证。......
我国医疗器械法规体系的构建始于2000年《医疗器械管理条例》的实施,经过2014年、2017年的2次修订后,法规体系的框架已经基本确立。根据......
3月26日,国务院新闻办公室举行《医疗器械监督管理条例》国务院政策例行吹风会,国家药监局副局长徐景和,司法部立法三局局长王振江,国家药监局......
......
开办第二类医疗器械生产企业必须具备以下条件:(一)企业负责人应具有中专以上学历或初级以上职称。......
......