在线客服
在线客服
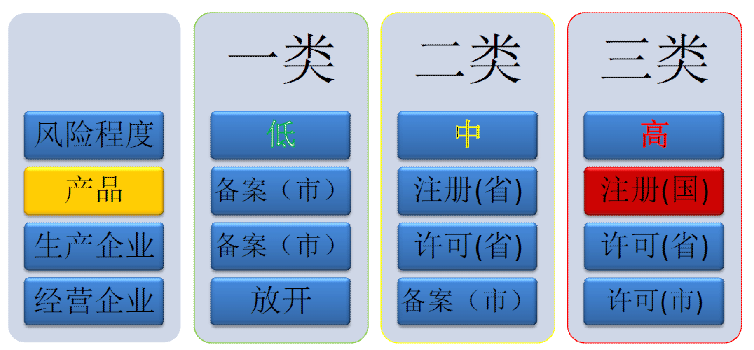
国内医疗器械注册分类管理,一张图告诉你!当产品被归类为中等复杂时,申请人认为其产品符合豁免标准,并可向FDA提交CLIA WAIVER申请。关于CLIA WAIVER申请,FDA有相关的指导文件。有兴趣的朋友可以查阅,不会在这里重复。指南名称是:ApplicationStudies对双510(k)和CLIA豁免的建议。
附录1记分卡标准(42 CFR 493.17)
记分卡分为7个测试,每个测试分为3个分数:1、 2、 3. 1是最低复杂度,3是最复杂的。测试后,将七个测试的分数加在一起。 12级及以下的级别是中度复杂的测试,12级以上的测试是非常复杂的测试。当特定测试的特征在描述的1到3之间时,该值被指定为2。
(1)国内医疗器械注册知识
(i)1分:(A)需要最少的科学和技术知识。 (B)可以通过工作描述获得操作所需的知识。
(ii)3分:在检查分析之前、分析、分析后需要专业知识。
(2)国内医疗器械注册培训和经验
(i)1分:(A)在分析、分析和分析后训练之前需要最少的训练。 (B)需要有限的经验
(ii)3分:(A)需要专业培训才能在、分析之前完成分析、分析后操作或(B)保证检测性能需要丰富的经验
国内医疗器械注册周期
- I类当场备案,但是现在大部分城市的药监局需备案者网上递交,通过初审才能去现场递交,无形中拉长了I类备案的时间。
- II类,93个工作日,这个只是药监局官方给的评审时间,且提交资料符合要求的情况下,如果资料不符合要求,会要求增补,周期会加长。
- III类,123个工作日,同样的,这是官方公布的初次评审的时间周期,根据具体的项目情况,注册周期会增加。
国内医疗器械注册费用
产I类不收取费用;
国产II类8-9万,各地药监局收费标准稍有不同;
国产III类15.36万;
进口I类不收取费用;
进口II类21.09万;
进口III类30.88万。
为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,根据《医疗器械注册与备案管理办法》(国家市场监督管理总局令第47号),国家药......
我国对于医疗器械有着严格的分类:一类,二类,三类!三类医疗器械是最高级别的医疗器械,也是必须严格控制的医疗器械,是指植入人体,用于支持、......
现在很多企业对于质量管理体系认证还是费是重视的,但是大多数企业还是一头雾水,对办理这个认证很模糊,今天小编就教大家如何准备质量管理体系的认证......
......
医疗器械的使用安全关系到广大患者的生命安全和健康,而医疗器械的使用安全则需要依靠相关法规的规范和监管。因此,医疗器械从业人员需要接受专业的医......
经营第一类医疗器械不需要备案,《医疗器械经营监督管理办法》第四条规定:按照医疗器械风险程度,医疗器械经营实施分类管理。经营第一类医疗器械不需......
进行医疗器械备案需要满足一系列的条件,包括申请人的资质、产品信息和资料、产品质量和服务体系、备案流程和要求等,以确保医疗器械的质量和安全性,......
广州安思泰企业管理咨询有限公司是一家专业从事国内医疗器械行业注册咨询公司,为客户提供专业的咨询服务,公司奉行“围绕法规、标准,专业服务客户,......
一类二类三类医疗器械有什么区别?一类医疗器械风险程度低,实行常规管理可以保证其安全、有效的医疗器械。二类医疗器械有中度风险,需要严格控制管理......
北京市药品监督管理局关于发布降低本市药品医疗器械产品注册收费标准的公告......